NGS药企合规服务:CAR-T慢病毒整合位点分析(LM-PCR扩增法)
近年来,嵌合抗原受体T(chimeric antigen receptor T,CAR-T)细胞疗法因在血液肿瘤中的突出疗效已成为肿瘤细胞免疫治疗领域中新的研发热点。但是该疗法所使用的慢病毒载体介导的基因转导可能存在一定的潜在风险:慢病毒在细胞基因组的整合可能引起原癌基因的激活、抑癌基因的失活、RNA 剪接、基因融合等,从而具有成瘤风险。根据国家药品监督管理局药品审批中心(CDE)发布的《基因修饰细胞治疗产品非临床研究与技术指导原则》,慢病毒外源序列在基因组的整合位点及安全风险评估是CDE放行的重要因素。
由此,针对CAR-T疗法中慢病毒改造的混合细胞,AZENTA自主创研、基于LM-PCR结合二代测序方法推出整合位点检测服务,可对整合位点相关基因进行功能分析,对整合位点偏好性画像,从而评估病毒载体的安全性。
LM-PCR全称为连接介导的PCR,我们采用了随机性更好的超声波法替代传统限制性酶切,将含有慢病毒插入的基因组进行随机打断并连接接头,然后通过两轮PCR富集含有慢病毒LTR-宿主区域的嵌合序列。对此扩增产物进行二代测序即可以分析确定载体在宿主基因组上的整合位点。
基于药企合规服务的高要求,我们对CAR-T慢病毒整合位点分析(LM-PCR扩增法)服务进行了升级:
- 引入reads的UMI矫正技术,位点判断更精确可靠;
- 增加测序数据饱和度分析,评估整合位点挖掘的全面性;
- 增加整合事件安全性评估相关分析,满足CDE申报需求;
- 基于分析结果,参考权威文献和CDE申报要求对结果进行总结并给出相应结论。
此外,我们还可以提供方法学验证,助力临床申报:
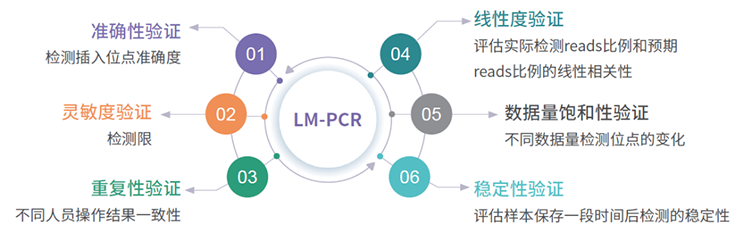
技术路线
实验流程包括核酸提取、DNA质量检测、基因组打断、LTR-host嵌合序列的LM-PCR富集、扩增子文库构建,以及上机测序等环节。在目标序列扩增和建库测序过程中,每一步实验的精准性与稳定性是保证后期生物信息分析结果可靠的必要条件。我们采用学术机构认可的品牌建库试剂与精确校准后的实验仪器,对实验过程的每个环节都进行高标准的质控,以获得高质量的测序数据。文库检测合格后,不同文库按照有效浓度及目标下机数据量的需求混样后进行测序。
基于测序完成获得的原始数据,生物信息分析过程主要包括以下步骤:
(1) 测序数据评估:过滤低质量序列,且只保留双端均可比对到宿主参考基因组的reads,统计数据量和数据质量等指标,数据质量满足分析要求后方可进行后续分析;
(2) 进行reads的UMI矫正与拼接,将成功拼接与未成功拼接的序列分别比对到宿主参考基因组;
(3) 整合位点检测:基于比对获得的结果进行整合位点的检测。
建库及分析流程如图所示:
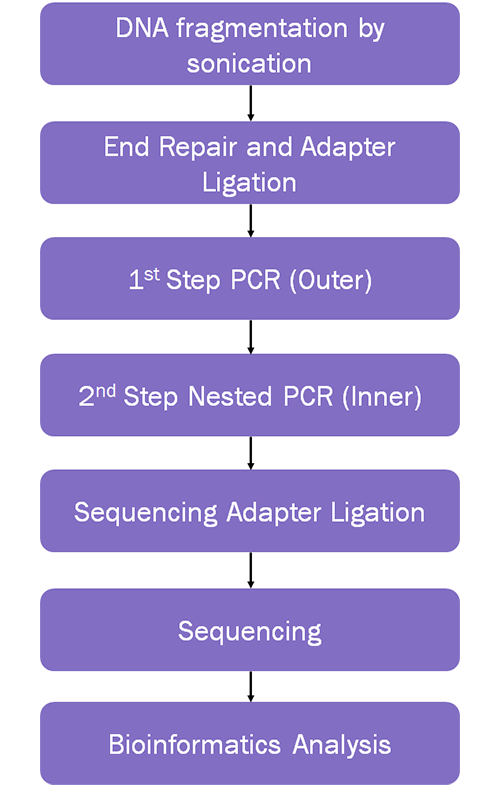
分析点介绍
首先,统计各样本整合位点数目,并基于refGene数据库的注释进行整合位点相关基因组功能区、CpG距离、TSS距离、Repeat class、CGC(Cancer Gene Census)、抑癌基因和致癌基因等信息的注释。基于以上整合事件注释结果,进行进一步的分析如下:
- 测序数据饱和度分析
测序数据量对于整合位点数据分析是非常重要的,通过进行饱和度分析,可以验证当前测序量能否满足需求,或者加大测序数据量是否能够进一步发掘更多的整合位点信息。
- 整合位点多样性分析
采用2种统计学指标来衡量整合事件在基因组上的分布多样性。
- 整合位点分布统计
统计展示位于TSS和CpG岛附近、位于基因组不同GC含量区间内和位于不同repeat区域的整合位点数目。通过测试发现,我们分析流程获得的TSS和CpG岛附近整合位点数据接近文献报道的检出情况,这也是整合事件安全性评估的重要指标之一。
- 整合位点安全性分析
一方面,展示整合位点位于肿瘤相关基因(致癌基因、抑癌基因)外显子区域的分布情况;另一方面,使用统计检验方法比较整合事件对于肿瘤相关基因和背景基因的偏好性。
结果展示如下:
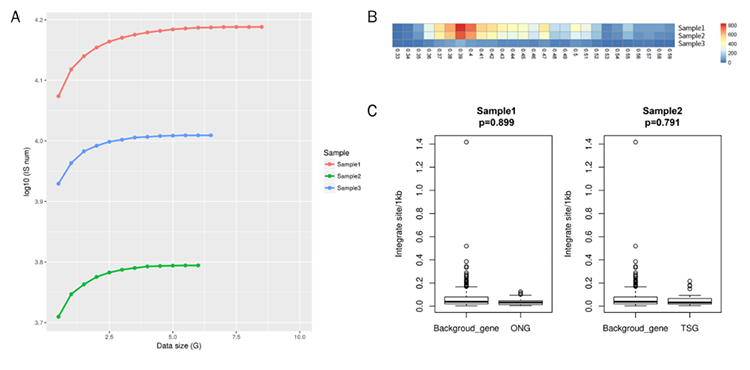
A. 测序数据饱和度分析;B. 插入位点在基因组不同GC含量区域的分布;C. 表达的原癌基因、抑癌基因与背景基因中的整合位点比较。
结语
CAR-T慢病毒整合位点分析(LM-PCR扩增法)是安升达推出的药企合规服务体系中重要的组成产品。可靠的检测方法可以有效分析重组细胞外源序列的整合位点,充分评估插入突变的可能性和相关风险,保证重组细胞安全性,从而为后续治疗效果评估提供保障,为顺利完成药品注册申报提供助力。
