CRISPR新应用—靶向整合DNA长片段(FiCAT)
近几年,随着CRISPR技术的发展和CGT(cell and genetherapy)领域的迅速扩张,研究者已经开始对人体内源细胞的基因进行编辑以治疗某些疾病。
2021年,两位CRISPR的技术先驱创立的基因治疗公司先后披露了基因编辑治疗的临床数据,张锋创立的Editas Medicine通过敲除基因CEP290的部分内含子序列来治疗Leber先天性黑蒙10型[1],Jennifer Doudna创立的Intellia Therapeutics则是通过移码突变基因TTR来治疗转甲状腺素蛋白淀粉样变性(ATTR)[2]。
另外,众多基因治疗公司都在进行的β-地中海贫血病和镰刀型贫血症的基因治疗,大多是通过突变BCL11A增强子,抑制基因BCL11A转录,来重新激活γ-珠蛋白的表达,替代突变的β-珠蛋白[3]。目前来看,首批进行人体内基因编辑治疗的临床实验,都选择了CRISPR的敲除功能,并设计较为稳妥的敲除方案,以达到疾病治疗的目的。
基因敲除只是CRISPR技术最为简单的一种应用,其造成的DNA双链断裂总是伴随着各种随机突变以及脱靶现象,细胞癌变的风险始终存在。从安全性的角度出发,基因治疗最终都会向序列精准编辑的方向发展。目前,不基于DNA双链断裂的碱基编辑和先导编辑已经在基因治疗中崭露头角,但这两类技术只能编辑较短的序列,目前仍然缺乏一类安全的定点长片段敲入技术用于基因治疗。
生物学界最常用的定点长片段敲入技术是基于DNA双链断裂的同源重组,其随机突变的安全性问题以及大片段同源重组的低效性问题,制约了它在基因治疗领域的发展。想要实现靶向整合基因的治疗方案,需要研究者在基因编辑技术上有新的突破。2019年发表的两篇文章在微生物中发现了天然存在的CRISPR转座子系统[4][5],提供了靶向整合长片段的一种新思路,不过目前该系统仍然只应用于原核系统,离临床应用有一定的距离。与此同时,也有研究者将CRISPR的靶向能力和转座子的整合能力进行人为组合,改造成为靶向整合DNA长片段的新技术。近期发表在Nature Communications的文章便是这一思路的产物,实现了最长9kbp的DNA片段的靶向整合[6]。

该技术被作者称为Find and cut-and-transfer(FiCAT),从原理图(图1)我们可以看出,作者希望借助Cas9的靶向定位能力,将常见的转座子PiggyBac定位到靶序列上,利用其高效的转座活性将长片段整合到靶序列上。
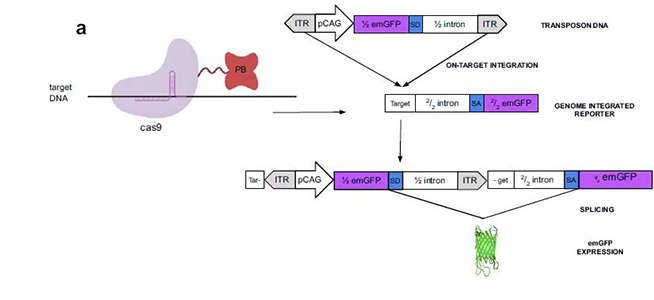
图1 FiCAT技术模型
在实际测试的过程中,作者对Cas9和转座酶PB都进行了优化,才实现了模型的设想。首先,PiggyBac的转座酶PB具有很强的随机位点转座的活性,Cas9的靶向作用并不能将整合限定在靶位点(图2),所以作者对转座酶PB进行了一系列的点突变筛选,才避免了脱靶的发生。

图2 FiCAT技术可以实现准确的靶向整合
但详细分析点突变的类型,我们会发现一些矛盾。这些点突变中,R372A和K375A降低了PB的DNA结合能力,能够降低随机位点的转座,提高其Cas9介导的靶向性;而D450N提高了转座酶去转座子的能力,实际上与定点整合是相违背的。作者接下来的筛选和分析中,对这个问题进行了一定的解释。在筛选转座酶点突变的同时,作者也对Cas9的形式进行了筛选(图3左),与设想不相符的是,酶活性位点突变后dCas9保留了DNA靶向结合能力,但与PB组合后,并没有实现靶向整合;反而是野生型Cas9与PB组合后,才观察到靶位点的整合。作者对靶向整合的边界序列的测序为这个异常现象提供了一定的解释(图3右)。PiggyBac转座子的边界序列是稳定不变的,但在FiCAT技术中,边界序列却很容易出现突变,并丧失了转座子序列再次转座的能力。这样边界序列发生突变的整合现象更像是非同源末端连接(NHEJ)介导的敲入,而非转座酶介导的转座现象,与作者预期的有些出入。这个现象也和前面转座酶的D450N点突变相印证,更强的去转座子能力可以让转座酶携带更多的转座子序列,用于NHEJ整合。
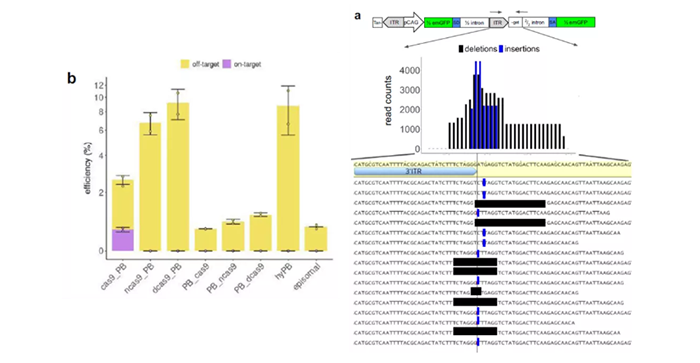
图3 FiCAT整合序列的边界并不稳定
虽然实际发生的过程并没有完全按照设想的模型进行,FiCAT技术还是实现了优于同源重组的靶向整合能力(图4左),在长达8kbp的超长序列敲入中优势尤为明显。对转座酶PB进行更深入的点突变筛选后,作者进一步提高了FiCAT技术的整合效率(图4右)。
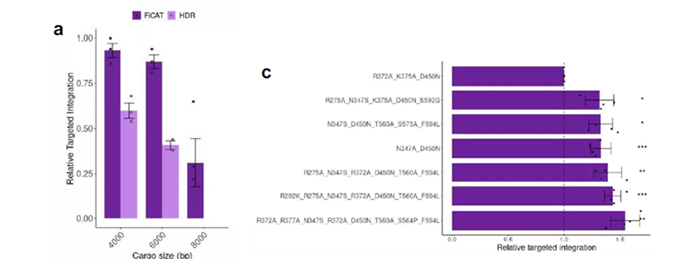
图4 FiCAT靶向整合大片段的能力优于同源重组
总结来说,这篇文章创造的技术FiCAT借助Cas9靶向结合和切割DNA双链的能力,将转座酶携带的转座子定点整合到靶序列上,但并没有利用到转座酶的整合能力,而是通过NHEJ机制将转座子序列连接到DNA双链断裂处。最终FiCAT技术相较于同源重组,在大片段的靶向整合上仍有着明显的优势。该技术为基因治疗提供了一种全新的思路,CRISPR系统和转座子系统的强强联合,很有可能成为基因编辑技术的一大发展趋势。该文章的作者 Dr. Marc Güell 和 Dr. Avencia Sánchez-Mejías 也凭借该技术在近期融资450万欧元,顺利进军基因治疗赛道[6],期待他们在临床领域的表现。
参考文献
[1]http://med.china.com.cn/content/pid/294276/tid/1026
[2]https://www.sohu.com/a/477993709_296660
[3]https://www.sohu.com/a/437101371_183834
[4]https://doi.org/10.1038/s41586-019-1323-z
[5]https://doi.org/10.1126/science.aax9181
[6]http://organicchem.com/show.asp?id=59331
